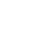La profesora del máster de Biotecnología UNIA/UMA, Ana Casañal, encabeza una investigación en la que se analiza el CPF, una maquinaria celular que actúa sobre el ARN mensajero, el cual contiene la información sobre la secuencia de aminoácidos que componen las proteínas.

En la actualidad en todos los centros educativos se imparten asignaturas que instruyen sobre la estructura y el funcionamiento de los componentes de la célula. Sin embargo, aun queda mucho por descubrir sobre su mecanismo, por lo que su estudio es el objetivo principal de muchos grupos científicos que buscan revelar en detalle la composición de las maquinarias celulares. Este es el trabajo que desempeña Ana Casañal, una profesora de la Universidad de Málaga (UMA) que desarrolla su labor investigadora en el MRC Laboratory of Molecular Biology en Cambridge. Allí la malagueña ha liderado el proyecto en el que, por primera vez, se ha visualizado a nivel atómico la estructura del Factor de Corte y Poliadenilación, más conocido por sus siglas en inglés CPF (Cleavage and
Polyadenylation Factor). Este compuesto se encarga de modificar y estabilizar el ARN (ácido nucleico que participa en la síntesis de las proteínas y realiza la función de mensajero de la información genética), producto directo de la descodificación del ADN, que determina en qué posición se colocan los aminoácidos para conformar las proteínas en el ribosoma.
“El buen funcionamiento de esta macromolécula es de gran importancia, ya que si no realiza correctamente su actividad, el organismo muere. Por otro lado, es la diana de muchas bacterias y virus que provocan diversas enfermedades. Estas pueden ser afecciones comunes u otras más inusuales como la beta talasemia, e incluso dolencias neurológicas. En este caso, hemos conseguido identificar una región de CPF a la que se puede unir una de las proteínas del virus de la gripe para afectar la expresión de genes en la célula”, explica la doctora.
Los avances en microscopia electrónica y en el proceso de preparación de muestra han sido clave para poder determinar por primera vez su morfología. “La criomicroscopía electrónica para la determinación estructural de biomoléculas en alta resolución ha sido vital para obtener modelos en 3D del CPF, entender su función esencial y ampliar el conocimiento sobre otros componentes fundamentales en la célula”, afirma Casañal.
Este innovador método, por el que Jacques Dubochet, Joachim Frank y Richard Henderson han sido galardonados con el Nobel de Química de 2017, consiste en congelar rápidamente la muestra a -190°C para así inmovilizar la proteína en su forma natural. El reconocimiento de este último no ha pillado por sorpresa a Casañal, que trabaja en el mismo lugar que Henderson y ambos colaboran a menudo en sus respectivos proyectos. Cabe destacar que el físico no es el único del centro que ostenta el título. Por los pasillos del laboratorio de la ciudad inglesa pasean 14 premios Nobel, al igual que lo hicieran en el pasado James Watson y Francis Crick, los cuales obtuvieron la prestigiosa distinción en 1962 por su descubrimiento de la doble hélice de ADN, que revolucionó el mundo de la genética.
Por su parte, la bioquímica ha aumentado el número de galardones de los integrantes del laboratorio. Casañal fue distinguida en junio de este mismo año con el premio FEBS al mejor póster en la Conferencia de Investigación Gordon, enfocada a avances en microscopia. Su trabajo presenta la morfología de CPF y las diferentes moléculas que los conforman, por medio de un dibujo en 3D. En este documento también se especifican los diferentes procesos de los que es responsable este complejo. “Ahora mismo estamos en el primer paso del estudio, que consiste en determinar la composición de esta multiproteína y desentrañar su estructura. Cuando sepamos todo sobre su configuración, podremos estudiar en detalle cómo y dónde es atacada por distintos microorganismos, como virus y bacterias , y así poder diseñar estrategias para combatir las enfermedades que producen”, explica la científica.
Además de su investigación en Cambridge, Ana Casañal también imparte el módulo de Biología Estructural del Máster de Biotecnología Avanzada UNIA/UMA. “En mi faceta docente, trato de que el alumno se familiarice con las diferentes herramientas para el análisis estructural de macromoléculas, poniendo especial atención en sus aplicaciones prácticas”, subraya la profesora.
Ana Casañal, Ananthanarayanan Kumar, Chris H. Hill, Ashley D. Easter, Paul Emsley, Gianluca Desgliesposti, Yuliya Gordiyenko, Balaji Santhanam, Jana Wolf, Katrin Wiederhold, Gillian L. Dornan, Mark Skehel, Carol V. Robinson, Lori A. Passmore (2017): “Architecture of eukaryotic mRNA 3’-end processing machinery”. Science, vol 358, pp. 1056-1059. Disponible en línea: https://doi.org/10.1126/science.aao6535